Malaria-Medikament hilft gegen Diabetes
Rund 15 Prozent der Zuckerkranken leiden an Typ-1-Diabetes, in Österreich sind das rund 40.000 Menschen. Ihre soeben erschienene Studie könnte ein Durchbruch in der Diabetesforschung sein, frohlocken die Forscher um Stefan Kubicek vom Forschungszentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften (CeMM).
Die Studie
„Artemisinins Target GABAA Receptor Signaling and Impair α Cell Identity“ , Cell, 1.12.16
Die Wirkung der Malaria-Medikamente konnten sie unter anderem an diabetischen Zebrafischen, Ratten und Mäusen zeigen: Deren Blutzuckerspiegel normalisierte sich. Da die Tiere den Menschen molekular ähnlich sind, könnten diese Effekte eventuell auch beim Menschen eintreten, hoffen die Forscher.
science.ORF.at: Die gegen Malaria zugelassene Wirkstoffgruppe der Artemisinine soll, quasi als Nebenwirkung, auch gegen Typ-1-Diabetes wirken, so Ihre neuesten Forschungsergebnisse. Was hat Sie zu dieser Erkenntnis geführt?
Stefan Kubicek: Wir wollten verstehen, was die verschiedenen Zelltypen ausmacht, die in der Bauchspeicheldrüse, genauer gesagt, in den dortigen Zellansammlungen namens Langehansscher Inseln, den Blutzuckerspiegel regulieren. Da gibt es mindestens fünf verschiedene Zelltypen, aber die bekanntesten davon sind sicherlich die insulinproduzierenden Betazellen.
Betazellen sind jene Zellen, die bei Typ-1-Diabetes durch eine Autoimmunreaktion zerstört werden. Das fehlende Insulin muss dann durch Injektionen ersetzt werden. Daneben gibt es auch noch einen anderen sehr wichtigen Zelltyp - die Alphazellen. Sie produzieren das Hormon Glukagon. Glukagon treibt den Blutzuckerspiegel nach oben, Insulin senkt ihn.

CeMM
Stefan Kubicek ist Leiter der Abteilung für Chemisches Screening am CeMM, der Österreichischen Plattform für Chemische Biologie (PLACEBO) und des Christian Doppler Labors für Chemische Epigenetik und Antiinfektiva.
Was aus früheren Forschungen bereits bekannt war: Die Alphazellen haben prinzipiell das Potenzial, sich in Betazellen umzuwandeln. Und zwar dann, wenn die Betazellen in großer Menge zerstört werden. Alphazellen verwandeln sich dann in Betazellen und produzieren plötzlich Insulin statt Glukagon. Eine Hauptrolle spielt bei diesem Umwandlungsprozess der Genschalter Arx in den Alphazellen. Wird er ausgeschaltet, beispielsweise durch Genmanipulation, setzt das den Umwandlungsprozess in Gang. Die fehlenden Alphazellen werden dann vom Körper erneuert. Wir haben uns gefragt: Gibt es vielleicht auch eine Substanz, die so eine Zellumwandlung auslösen könnte? Und hier sind wir bei Artemisininen fündig geworden.
Es war also ein Zufallsfund?
Hier am CeMM haben wir über 90.000 Substanzen zu Testzwecken eingelagert - unsere „Substanzbibliothek“. Darunter sind unbekannte Substanzen, aber auch bereits zugelassene Medikamentenwirkstoffe. Wir hatten keine Hypothese, die uns Artemisinine speziell testen ließ, sondern wir haben wirklich alle Substanzklassen der zugelassenen Medikamente an Alphazellkulturen durchgetestet und sind so auf die Artemisinine gestoßen. Artemisinine blockieren den genetischen Schalter Arx indirekt. Die Alphazellen produzieren dann Insulin statt Glukose.
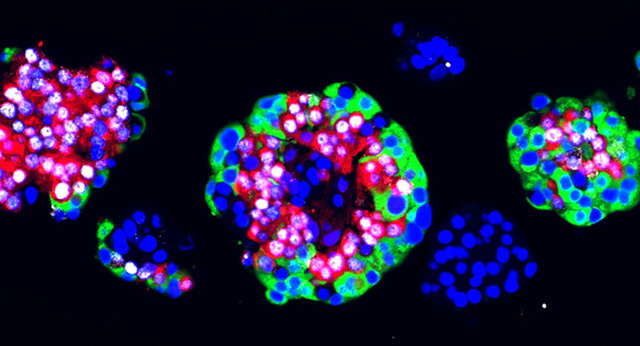
Cell Press
Menschliche Langehanssche Inseln unter dem Mikroskop, mit Artemisinin behandelt und immunofluoreszent gefärbt: Zellkern (blau), Arx (weiß), Glukagon (rot) und C-Peptid (grün)
Können wir Artemisinine nun ganz praktisch auch bei Diabetes anwenden?
Bis dahin ist es noch ein weiter Weg. Zunächst einmal müssen wir zwei Dinge ausschließen: Erstens, dass auch die neu gebildeten Betazellen wieder vom Körper selbst zerstört werden - schließlich ist Typ-1-Diabetes eine Autoimmunerkrankung. Und zweitens müssen wir sichergehen, dass die Alphazellen auch langfristig regenerationsfähig bleiben, ihre Anzahl also trotz der ständigen Umwandlung in Betazellen nicht abnimmt. In unseren Tierversuchen - mit diabetischen Zebrafischen, Mäusen und Ratten, hat das bisher gut funktioniert.
Ö1-Sendungshinweis
Über das Thema berichtet auch das Ö1-Morgenjournal, 2. Dezember, 7.00 Uhr.
Aber auch das Medikament selbst muss auf Langzeitanwendung neu getestet werden: Es ist zugelassen für die Behandlung von Malaria, und da ist ein sehr kurzer Behandlungszyklus notwendig. Typischerweise werden Artemisinine für vier Tage gegeben. Um eine ordentliche Umwandlung von Alpha- in Betazellen hervorzurufen, brauchen wir aber wesentlich längere Behandlungszeiträume. Ob dann unerwünschte Nebeneffekte oder Vergiftungen auftreten, muss in klinischen Studien erst noch gezeigt werden.
Das Medikament selbst könnte aber in seiner jetzigen Form verabreicht werden?
Eher nicht: Diese Artemisinine haben ein paar unerwünschte physikochemische Eigenschaften. Sie sind sehr schlecht wasserlöslich und haben eine sehr kurze Halbwertszeit im Plasma. Bei Malaria, einer akut lebensbedrohlichen Erkrankung, kann man natürlich alle paar Stunden eine neue Artemisinine-Dosis geben. Das ist aber langfristig, also für chronische Erkrankungen wie Diabetes, weniger wünschenswert. Es wird wohl nötig sein, die Formulierungen von Artemisinine so zu verändern, dass sie auch langfristig abgegeben werden können.
Wie lange wird es dauern, bis wir Artemisinine als Medikament gegen Typ-1-Diabetes wirklich anwenden können?
Bekannt ist ja, dass die Medikamentenentwicklung sehr lange dauert. Zehn Jahre sind etwa zur Entwicklung von neuen Medikamenten nicht ungewöhnlich. Bei Artemisininen handelt es sich um eine bereits zugelassene Wirkstoffgruppe, also, hoffentlich kann man hier ein paar Jahre abkürzen. Fünf Jahre wären ein wünschenswertes, zugleich auch realistisches Ziel.
Hanna Ronzheimer, Ö1 Wissenschaft

