Warum geplatzte Blutzellen Bakterien sprießen lassen
Bisher galt Eisen als Hauptverdächtiger: Als zentraler Bestandteil des Häms im Blutfarbstoff Hämoglobin verleiht das Metall den roten Blutkörperchen ihre Farbe und die Fähigkeit, Sauerstoff zu transportieren – doch es ist auch ein wichtiger Nährstoff für Bakterien.
Studie
”Heme drives hemolysis-induced susceptibility to infection via disruption of phagocyte functions“, Nature Immunology, 31.10.16
Sylvia Knapp vom Forschungszentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften (CeMM) und der Meduni Wien widerlegt mit ihrem Forschungsteam nun dieses Dogma. Häm dient demnach nicht als Bakterienfutter, sondern lähmt Immunzellen.
Immunzellen verkrampfen
„Wir konnten im Reagenzglas und im Mausversuch zeigen, dass das Bakterienwachstum in den meisten Fällen nicht von dem Eisen im Häm abhängt“, erklärt Rui Martins, Erstautor der Studie, in einer Aussendung. „Stattdessen fanden wir heraus, dass Häm die Makrophagen bewegungsunfähig macht - diese Fresszellen sind eine der wichtigsten Immunzellarten für die Bakterienabwehr“.
Das Häm-Molekül bringt das Cytoskelett der Makrophagen durcheinander und nimmt den Zellen dadurch ihre Beweglichkeit. „Es erinnert an einen Muskelkrampf, die Zellen werden innerhalb von drei Minuten komplett bewegungsunfähig“, beschrieb Martins die Wirkung des Häms.
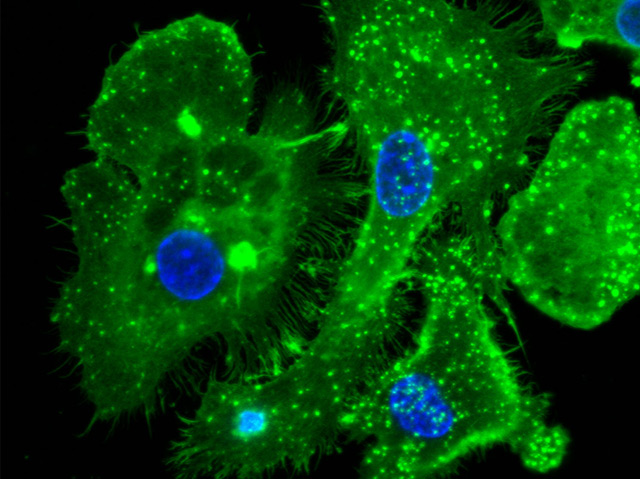
CeMM/Rui Martins
Unter dem Mikroskop: Menschliche Makrophagen, zehn Minuten lang zehn Mikrometer großen Häm ausgesetzt
Das Cytoskelett ist für die Beweglichkeit der Fresszellen entscheidend: Es besteht aus langen, verzweigten Fasern, die sich wie ein Gerüst durch die gesamte Zelle ziehen. Durch gezielten Auf-und Abbau dieser Fasern kann die Zelle in bestimmte Richtungen „wachsen“, um sich beispielsweise ein eindringendes Bakterium einzuverleiben.
Doch dafür ist ein fein abgestimmtes genetisches Programm nötig, in dem das Protein DOCK8 eine zentrale Rolle spielt. „Durch biochemische Versuche haben wir herausgefunden, dass Häm sich mit DOCK8 verbindet und es dauerhaft aktiviert“, sagte Sylvia Knapp. Dadurch geht die Kontrolle über das Cytoskelett verloren - die Fasern wuchern in alle Richtungen und legen die Zelle lahm.
Chinin als mögliches Gegenmittel
Das Resultat: Bakterien können sich praktisch ungehindert vermehren. Das dürfte bei Millionen Menschen der Fall sein, welche im Rahmen anderer Erkrankungen an Hämolyse leiden: bei Sichelzellanämie, Malariainfektionen oder Beta-Thalassämie.
Die neuen Erkenntnisse könnten auch zu einem Gegenmittel führen. "Chinin, das zur Behandlung von Malaria eingesetzt wird und von dem man bereits vermutete, dass es an Häm bindet, blockiert auch die Verbindung mit DOCK8, sagte Knapp. „Wir zeigen damit, dass es tatsächlich möglich ist, Immunzellen zu ‚reaktivieren‘ und die Immunabwehr gegen Bakterien bei Patienten mit Hämolyse wiederherzustellen.“
science.ORF.at/APA

