„Genschere“ heilt Erbkrankheit
Die Wissenschaftler um den Biologen Shoukhrat Mitalipov von der Oregon Health & Science University haben in ihren Laborversuchen ein recht konkretes Szenario durchgespielt. Es lautet: Ein Mann mit der genetischen Anlage für eine Herzkrankheit will mit seiner Frau ein Kind bekommen. Bei einer natürlichen Befruchtung beträgt die Wahrscheinlichkeit, dass die Kinder ebenfalls von der gefährlichen Krankheit betroffen sind, 50 Prozent.
Studie
„Correction of a Pathogenic Gene Mutation in Human Embryos“, Nature (2.8.2017).
Therapie im Reagenzglas
Das Team um Mitalipov griff allerdings in die Verschmelzung von Spermien und Eizelle ein. Mit Hilfe der Gen-Editierungsmethode CRISPR/Cas gelang es ihnen, den Prozentsatz gesunder Embryonen auf 72 Prozent zu steigern.
Bei der dergestalt behandelten Krankheit handelt es sich um eine erbliche bedingte Herzmuskelschwäche (Familiäre Hypertrophe Kardiomyopathie). Sie erhöht das Risiko für plötzlichen Herztod - auch bei jungen Patienten - und ist durchaus häufig: Die entsprechende Mutation tragen zwei von tausend Menschen in ihrem Erbgut.
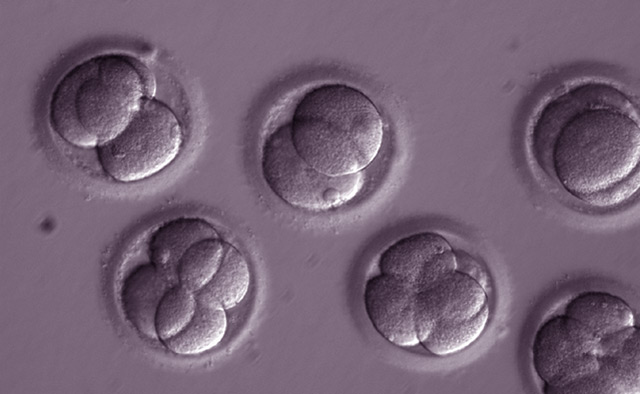
OHSU
Die menschlichen Embyonen zwei Tage nach der Behandlung
Mitalipov betrachtet seine Versuche als Weg, „Familien von der Bürde dieser Erbkrankheit zu befreien“. Auch deshalb, weil bei dem Eingriff offenbar keine unerwünschten Nebeneffekte aufgetreten sind. Ob CRISPR/Cas tatsächlich so sicher ist, wie von den Forschern behauptet, ist allerdings noch nicht hinreichend geklärt. Amerikanische Mediziner hatten etwa im Juni dieses Jahres darauf hingewiesen, dass beim „Gene-Editing“ sehr wohl Mutationen mit unabsehbaren Wirkungen auftreten könnten.
Ziel: Genetisch kurierte Kinder
Die Versuche fanden wohlgemerkt im Reagenzglas statt. Ein Kind hätte sich aus den Embryonen nicht entwickeln können. Genau das ist jedoch das Ziel von Mitalipov. Er will die Methode in Zukunft bei künstlichen Befruchtungen einsetzen, die Anwendungsbereiche wären vielfältig: Sie reichen von der Vorbeugung von Brustkrebs bis hin zur Behebung von Stoffwechseldefekten.
Freilich unter der Voraussetzung, dass sich die Methode als ebenso sicher wie treffsicher erweist. Damit man sich an klinische Versuche am Menschen (also die Einpflanzung von gentechnisch veränderten Embryonen in die Gebärmutter) heranwagen könnte, müsste „die Trefferrate 90 bis 100 Prozent betragen“.
Zweite Voraussetzung wäre eine rechtliche Basis für derartige Versuche. Hier ist die Lage international sehr unterschiedlich. In Österreich verbietet etwa das Fortpflanzungsmedizingesetz Eingriffe in das Erbgut von Embryonen, selbst wenn sie nur im Reagenzglas stattfinden.
Länder wie die USA und China sind da deutlich liberaler. Doch zumindest auch in den USA wären klinische Versuche am Menschen nicht ohne zusätzliche Genehmigungen oder sogar Gesetzesänderungen erlaubt, wie Mitalipov bei einer Pressekonferenz der Zeitschrift „Nature“ betonte. Wann es dazu kommen könnte, sei gegenwärtig nicht abzuschätzen.
Auf dem Weg zum „Designerbaby“?
Bei der Debatte über die Zulassung von Keimbahntherapien geht es nicht nur um Fragen der medizinischen Sicherheit und Angemessenheit, sondern auch um einen möglichen Missbrauch der Methode. Wenn es möglich ist, schädliche Gene auszutauschen, dann ist es im Prinzip auch möglich, erwünschte Eigenschaften ins Erbgut zu schleusen. So gesehen könnten derartige Versuche auch den Weg zum „Designerbaby“ ebnen.
Christiane Druml, die Vorsitzende der Österreichischen Bioethikkommission, hält das gegenwärtig für eine „virtuelle Debatte“. Solange man die Gene für „Schönheit, Sportlichkeit, Musikalität und Intelligenz“ nicht kenne und entsprechend zu manipulieren wisse, sei es zu früh, darüber zu spekulieren. „Der Begriff ‚Designerbaby‘ führt die Debatte in eine semantisch falsche Richtung. Es geht derzeit nur um Menschen mit Erbkrankheiten, die keine gesunden Kinder bekommen können.“
Die galoppierende Entwicklung kritischer betrachtet indes Christiane Woopen, Vorsitzende des Europäischen Ethikrates. Sie bemängelt, die Forscher gingen wie selbstverständlich davon aus, dass die Methode am Menschen angewendet werden soll. "Sollte das Wettrennen um den größten Ruhm und die einträglichsten Patente wichtiger sein als die Verständigung darüber, ob die Weltgemeinschaft einen redaktionellen Eingriff in das ‚genetische Buch des Lebens’ befürwortet?“
Woopen plädiert dafür, zunächst einmal die Grenzen der Forschung international festzulegen - und erst dann mit solchen Experimenten fortzufahren. Dass das im kompetitiven System namens „Wissenschaft“ tatsächlich passieren wird, ist nicht sonderlich wahrscheinlich.
Robert Czepel, science.ORF.at

